“科技与人文”系列
2018年12月13日晚上,“北大文研论坛”第八十七期在北京大学静园二院208会议室举行,主题为“基因编辑与科学伦理”。北京大学生命科学学院院长吴虹主持,北京大学生命科学学院魏文胜研究员、邓宏魁教授、汤富酬教授,北京大学哲学系刘哲副教授参与讨论。文研院院长邓小南教授出席。
活动开始后,吴虹教授首先介绍了活动的缘起和本次论坛的结构安排。吴虹教授表示,在科学研究领域,基因编辑技术已经取得了若干重大突破。然而,这一技术的应用在伦理层面具有潜在的风险,近期的基因编辑婴儿事件也引发了公众广泛的讨论。本次论坛邀请到该领域顶尖的科学家和人文学者,旨在帮助公众梳理基因编辑的背后的科学伦理和社会伦理。吴虹教授表示,基因编辑技术在科学层面有三个主要问题:CRISPR/Cas9基因编辑技术、CCR5基因以及生殖细胞和胚胎发育。三位生命科学家将分别对这三个问题进行介绍。随后,刘哲副教授将对基因编辑技术的应用涉及的社会伦理进行阐释。
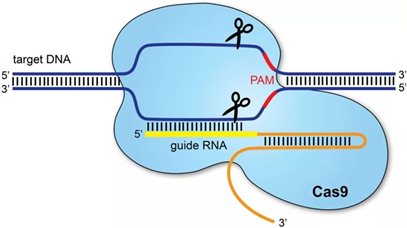
第一位发言者魏文胜研究员简述了CRISPR/Cas(clustered regularly interspaced short palindromic repeats/CRISPR associated)的发现、在生命体中的作用和目前在其研究和应用的前沿问题。

首先,魏文胜研究员介绍了生命科学中精准诊断(precision diagnosis)和精准医疗(precision therapy)这两个概念。他表示,前者与基因测序有关,用于解读生命现象与遗传密码之间的逻辑关系。后者既可指通过获得精确的信息对个体进行相应的治疗,也可指通过基因编辑技术对基因进行“改写”。魏文胜研究员认为,“写”的难度远高于“读”。而在基因编辑技术中,定位到需要“写”的基因比基因编辑操作更困难。
其次,魏文胜研究员介绍了CRISPR/Cas系统。他表示,天然的CRISPR/Cas系统广泛存在于细菌和古细菌,它是微生物的免疫系统,可以帮助细菌抵御病毒入侵。同时,该系统为细菌提供了获得性免疫,当细菌遭受病毒入侵时,会产生相应的“记忆”。当病毒二次入侵时,CRISPR系统可以识别出外源DNA,并将它们切断,沉默外源基因的表达,从而抵抗病毒的干扰。正是由于这种精确的靶向功能,同时相关操作的实验门槛较低,CRISPR/Cas系统被开发成一种高效的基因编辑工具。

早在1932年出版的小说《美丽新世界》(Brave New World)中,阿道司·赫胥黎(Aldous Huxley)就构筑了一个反乌托邦的未来世界——人类从遗传和基因上就已经被先天设计为各种等级的社会成员,自由和个性被扼杀
再者,魏文胜研究员介绍了基因编辑技术的应用情景。他表示,生命科学研究的是生命现象与遗传密码之间的因果关系,基因编辑技术使得人类在基因水平上的认知更进一步,在新药研发、物种培育、畜牧业等方方面面有着广泛的应用。特别值得一提的是,基因编辑技术在治疗地中海贫血、艾滋病和癌症等疑难杂症方面有着广阔的前景。最后,魏文胜研究员提出了基因编辑中的科学问题和伦理问题。他表示,基因编辑技术是一把双刃剑,需要在中靶效率和脱靶效应之间找到平衡。他提出,禁止对生殖细胞进行基因编辑是目前生命科学工作者达成的共识。科学工作者如果逾越这条红线,滥用基因编辑技术,很可能会引起公众的恐慌和监管部门对相关领域研究和应用的收紧。
第二位发言的是邓宏魁教授。他介绍了CCR5基因的发现、生物学功能及其在艾滋病治疗和预防中的应用。首先,邓宏魁教授介绍了CCR5基因的发现及其生物学功能。邓宏魁教授表示,CCR5基因的发现具有重要的科学意义,这一发现被《科学》杂志评为1996年十大科学发现之首。CCR5基因是趋化因子受体的一种,可以参与炎症反应并与HIV表面蛋白gp120结合,并帮助HIV进入T细胞。因此,CCR5也被称为HIV攻击T细胞的“帮凶”。
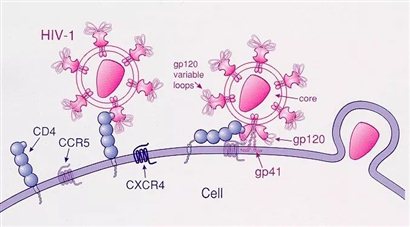
CCR5, 趋化因子受体的一种,是MIP 1α,1β,和 RANTES的受体。参与炎症反应,与HIV表面蛋白•gp120结合,帮助HIV进入T细胞
接着,邓宏魁教授介绍了CCR5△32这一天然的抵抗HIV的突变体。研究者对2位反复暴露于HIV却不受感染的健康人进行研究后发现,他们体内的CCR5(当时称为CKR5)基因存在32bp碱基缺失,并将其称为 CCR5△32突变体。此外,研究发现,在欧洲人种中CCR5△32突变比例高达14%。研究者认为,CCR5△32在欧洲人种中的高突变率或为正向选择的结果——自然状态下,单基因突变体占据人群10%以上至少需要12万年,而CCR5△32突变只用了2500年就做到了。因此,环境中必然存在正向选择将CCR5△32突变体富集起来。研究者推测,在东地中海文明时期(公元前1500年至公元744年)频繁爆发的出血热(hemorrhagic fevers)或为最可能的CCR5△32突变选择方式。那么,CCR5基因突变是否存在潜在风险?邓宏魁教授介绍了现有研究中的主要发现:美国患者基因分析表明,CCR5Δ32突变人群西尼罗病毒(West Nile virus)感染风险增大;人群中蜱媒脑炎(Tickborne Encephalitis)的严重程度和CCR5Δ32突变的比例呈正相关;欧洲患者基因分析表明,CCR5Δ32突变人群的流感致死率是正常人群的3倍。

出血热(hemorrhagic fevers)最可能的CCR5△32突变选择方式。它由RNA病毒造成的传染病,以发烧及出血为典型病征,在东地中海文明时期(公元前1500年-公元744年)频繁爆发
接下来,邓宏魁教授解释了通过敲除CCR5基因使人体抵抗艾滋病的原理和具体策略。首先,他介绍了世界上第一个(也是唯一一个)被公认治愈的艾滋病患者蒂莫西·布朗(Timothy Brown)的经历及其对艾滋病治疗的启发。布朗先后确诊患有艾滋病和急性髓细胞性白血病。受关于CCR5△32研究的启发,布朗的白血病主治医师格罗·修特(Gero Huetter)设想,如果能找到一个带有纯合CCR5Δ32变异的供体,把其骨髓移植给布朗,新生的免疫系统就能够免于HIV病毒的侵袭,即可帮助布朗同时治愈白血病和艾滋病。幸运的是,医生从骨髓库360万名捐献志愿者中找到267名合适的供体,并在检测到第61名供体基因时终于找到了带有纯合Δ32变异的供体。在接受骨髓移植后仅2月,布朗体内血液细胞都具备CCR5Δ32变异;移植后3个月,布朗血液中再也检测不到HIV病毒,且CD4+T淋巴细胞等反应机体免疫力的关键指标持续上升,最终痊愈。

“柏林病人”蒂莫西·布朗(Timothy Brown),世界上第一个也是唯一一个公认治愈的艾滋病人
邓宏魁教授表示,上述事例表明,通过基因编辑技术改变CCR5结构,使机体抵抗HIV感染是可行的,而这需要细胞来源和基因编辑工具这两个要素。具体来说,通过基因编辑获得CCR5基因缺失的造血干细胞,再将其植入HIV患者体内,则可以源源不断地提供CCR5缺失的T细胞,而CRISPR-Cas9的发现则提供了高效的基因编辑工具。随后,他介绍了临床动物实验中通过敲除造血干细胞中的CCR5基因治疗艾滋病的具体策略。第一步,利用CRISPR敲除人造血干细胞的CCR5基因;第二步,将经过基因编辑的造血干细胞移植到实验动物体内;第三步,检测造血干细胞功能的完整性;第四步,检测移植受体的抵抗HIV的能力;第五步,临床试验。已有实验表明,敲除CCR5基因的造血干细胞移植受体能抵抗HIV感染。最后,邓宏魁教授提出,通过成体细胞的基因编辑来治愈艾滋病是可行的——利用基因编辑技术获得CCR5基因突变的造血干细胞,使其源源不断提供CCR5基因突变的T细胞,以抵抗HIV侵染。
CRISPR-Cas9——基因编辑工具
第三位发言的是汤富酬教授。他介绍了早期胚胎发育中生殖细胞和体细胞的分化以及基因编辑对个体和遗传的影响。首先,汤富酬教授强调了人类生殖细胞(Germline cell)对于人类物种延续的重要性。他表示,人体约有40万亿个细胞,但真正传给下一代的是一个生殖细胞中的一半的遗传物质——来自父方的精子和母方的卵细胞结合形成受精卵,逐渐发育成胚胎,最终发育成为胎儿,胎儿也会形成生殖细胞。如此循环,人类物种得以延续。接着,汤富酬教授解释了为何目前只能对体细胞进行基因编辑,而不能对生殖细胞进行操作。他表示,对成体细胞进行基因编辑操作帮助患者治疗重大疾病只会对个体造成影响。如果对生殖细胞进行基因编辑操作,该基因会传给下一代,进入人类基因库。此外,由于基因是多效的,当对某个基因进行编辑后,可能带来预料之外的后果。随着携带该基因的个体的交配和繁衍,该变异基因会对多个人乃至群体产生不可控的影响。
第四位发言者刘哲副教授从生命伦理和生命政治的角度发表了自己的看法。刘哲副教授首先介绍了生命伦理和生命政治的概念以及二者之间复杂的联系。他表示,虽然生命伦理走向制度化只有四、五十年的历史,但发展得非常迅速。早先,生命伦理主要是指由科学家和医生们组成的行会体系构建起来医学伦理。数十年来,科学工作者的职责、监管范围、监管平台所依托的职业关系体系都发生着深刻的变化。关于生命政治,刘哲副教授主要引述了福柯的论述。在福柯看来,生命政治包含了三个重要的部分。第一部分是专家和学者,他们向公众传授知识并构建公共话语。第二部分是影响监管策略和干预策略制定的机制。这些干预策略可以来自国家、学校教育或和健康产业相关的机构(如保险公司、慈善机构等)。第三部分是个体对于监管和规训的内化。刘哲副教授认为,当个体以个人健康、家庭健康或者群体健康的名义把监管和规训纳入到对于自身理解当中,它们就不再是外在的。这三个部分共同构成了身体意义下个体本身的监管机制。刘哲副教授表示,生命政治与生命伦理并存发展,二者之间的关系十分复杂,至今还是一个开放的理论研究的话题。生命伦理如何构建我们的生命政治,反过来,生命政治又如何影响我们对于生命伦理的理解,都是值得继续思考的话题。

1999年的电影《黑客帝国》(The Matrix)中,人类由机器在“母体”中培育而来
接下来,刘哲副教授介绍了《纽伦堡守则》、《赫尔辛基宣言》和《生命医学伦理原则》等在生命伦理发展过程中具有重要意义的文本。1947年,《纽伦堡守则》针对纳粹于战时对人类进行不人道的实验而制定,强调自愿同意(voluntary consent)和自由选择的权力(free power of choice)。1964年发表的《赫尔辛基宣言》则非常明确地对知情以及知情的内容作了规定,并且要求同意必须以书面成文的形式呈现。刘哲副教授表示,从上世纪80年代以来,呼吁保护患者和被试者权益的声音越来越多,在此背景下出版的《生命医学伦理原则》成为了美国医学院的科研伦理教学中普遍使用的教科书。该书介绍了美国的生命伦理的四个重要原则,即:自主原则、惠济原则、不伤害原则以及正义原则。刘哲副教授表示,尽管在该书出版时,学界对上述四个原则的优先级曾存在争议,但是自九十年代后,自主原则已经占了上风。为了阐述自主选择的意涵,他引述了约翰·斯图尔特·密尔(John Stuart Mill)的著名论述。密尔认为,个体的自由是最大可能地实现最大多数人的善的基石。刘哲副教授表示,在讨论个体自由的时候,密尔谈到了三个方面:第一,个体自由意味着人有自己的个性和进行选择的自由;第二,个体的选择并不是为所欲为,而是需要考虑同类,不能伤害周围其他人选择的自由;第三,政府和公共社会对于个体的选择也会有约束和限制。

《生命医学伦理原则》(Principles of Biomedical Ethics)书影
随后,刘哲副教授讨论了生命伦理学家在公共讨论中的角色。第一,生命伦理曾局限于科学家和医生组成的行会内部,但在过去几十年间,生命伦理学家的话语权在逐渐增强。第二,生命伦理学家的角色是帮助患者和被试者争取他们的权益,重塑自我认知,使得他们将自己理解为有权利的利益相关方,而不是被动接受的个体。第三,近年来,律师、哲学家、神学家等非生命科学专家逐渐进入到政府的监管部门,为新兴的科技实验、临床应用制定指南。以上世纪九十年代末法国成立的反疾病法国联盟为例,刘哲副教授论述了在生命伦理不断发展的背景下,人们从身份认同到基因认同的转变。该联盟成立的初衷为因基因缺失而患肌蛋白萎缩疾病的患者争取权益。当时,法国政府对于相关疾病的关注和投资不足,但患者们认为,科研支持和医学治疗是自己应该享有的公民权利,因而组织起来表达抗议。刘哲副教授认为,这意味着人们开始将公民身份同生命权、健康权和救治权联系在一起,而不是将公民身份等同于抽象的政治信念。
最后,刘哲副教授介绍了生命经济及其与生命伦理的关系。首先,他表示,生命经济是指将身体作为开发利用的对象的新兴经济。借助生物科技的发展,生命经济由器官层面扩展到分子水平,基因也成为可以存储、挪动和编辑的对象。刘哲副教授表示,从某种意义上来说,生命经济使我们的身体失去了原有的专属性和完整性,变成了可以分离和提取的各个部分。其次,刘哲副教授认为,生命经济兴起和发展的背后除了技术的进步,还有资本运作和政治的影响,多种因素共同构成了生命经济的循环。他表示,这一循环对关于道德生命本身的传统的概念框架和理论假设提出了挑战和颠覆,增加了道德地位认证的模糊性。在此背景下,生命伦理变得非常重要,它可以帮助人们对资本的流动进行价值判断和管控。再者,刘哲副教授表示,在当代的生命政治结构当中,个体已经在赋权运动中重塑了自我认知,不再把自己作为生命技术的被动接受者,而是一个积极的行动者。同时,人们的选择会受到公共话语和公共知识的影响,而人们的目标是为了自己的身体拥有更好的未来。从这个意义上讲,他认为生命经济也是有希望的经济学。

弱势和边缘群体的声音,依然需要社会的关注
提问环节,有观众提问,基因编辑和自然突变带来的基因变异有何不同,以及除了治疗疾病,基因编辑的使用范围是否可扩展到增强人体的某些功能。汤富酬教授认为,自然突变是不可避免的,但是通过人为干预来增强特定功能是不可以的。目前科学界的共识是,除了治疗严重疾病,基因编辑技术不能用于强干预人的生命。魏文胜研究员表示,基因编辑是人为的,它对基因的改变是自然进化速度的千倍万倍。此外,他认为伦理问题具有复杂性,如何定义“增强”值得进一步探讨。即使假设基因编辑的修改是精准的、基因的功能是单一,仍存在着很多伦理争议,如基因编辑的受试是否有生育下一代的权利。邓宏魁教授认为,从免疫学的角度来考虑,通过基因编辑技术对人体基因进行强干预有可能破坏人类基因的多样性,造成群体对病毒免疫力的下降。